Параграф 26 Вопрос 5 ГДЗ Габриелян 9 класс (учебник 2020г) (Химия)
Решение #1

Рассмотрим вариант решения задания из учебника Габриелян 9 класс, Дрофа, Просвещение:
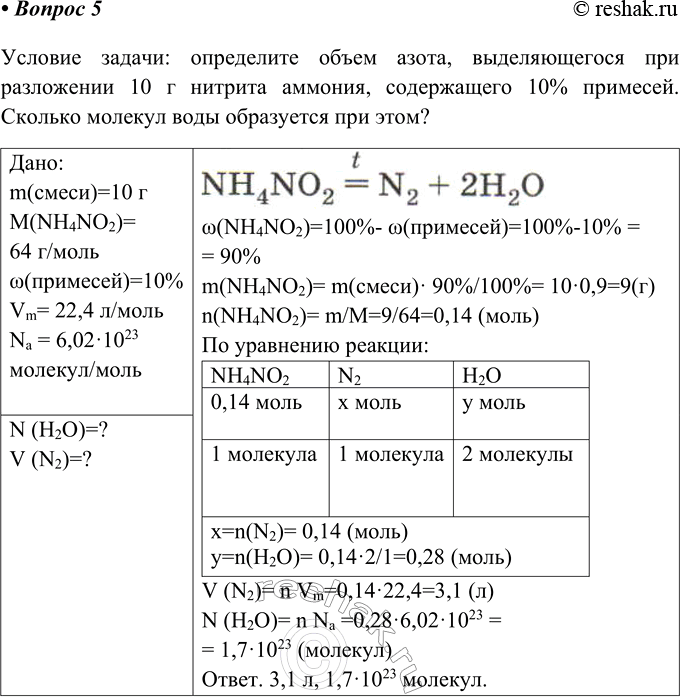
5 В лаборатории азот получают разложением нитрита аммония: NH4NO2 = N2+ 2Н2О.
Придумайте и решите задачу, в условии которой была бы указана масса исходного вещества и массовая доля в нём примесей, а требовалось бы найти объём одного продукта и число молекул другого получаемого вещества.
Условие задачи: определите объем азота, выделяющегося при разложении 10 г нитрита аммония, содержащего 10% примесей. Сколько молекул воды образуется при этом?
Дано:
m(смеси)=10 г
M(NH4NO2)= 64 г/моль
w(примесей)=10%
Vm= 22,4 л/моль
Na = 6,02·1023 молекул/моль
N (H2O)=?
V (N2)=?
w(NH4NO2)=100%- w(примесей)=100%-10% = 90%
m(NH4NO2)= m(смеси)· 90%/100%= 10·0,9=9(г)
n(NH4NO2)= m/M=9/64=0,14 (моль)
V (N2)= n Vm=0,14·22,4=3,1 (л)
N (H2O)= n Na =0,28·6,02·1023 = 1,7·1023 (молекул)
Ответ. 3,1 л, 1,7·1023 молекул.
Похожие решебники
Популярные решебники 9 класс Все решебники
*размещая тексты в комментариях ниже, вы автоматически соглашаетесь с пользовательским соглашением









