Страницы 135-136 ГДЗ Рабочая тетрадь Габриелян 8 класс (Химия)

Рассмотрим вариант решения задания из учебника Габриелян 8 класс, Дрофа:
РАСЧЁТЫ ПО ХИМИЧЕСКИМ УРАВНЕНИЯМ
Часть I
2. Рассмотрим пример.
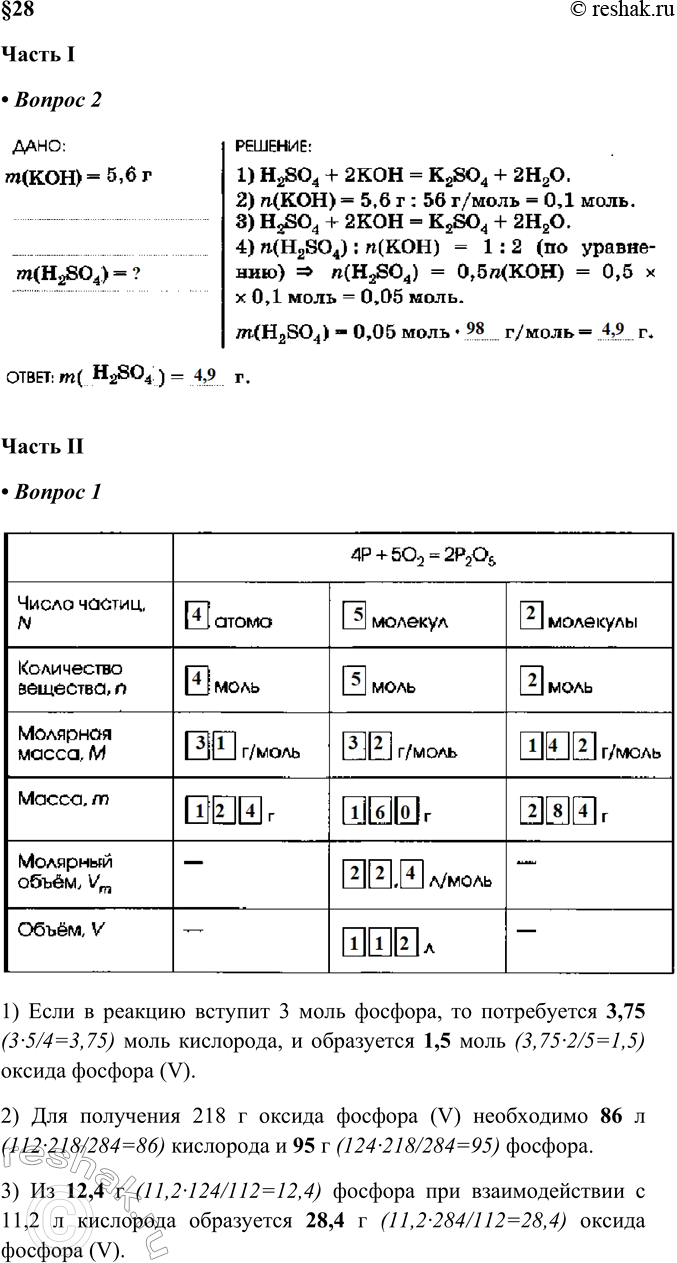
Рассчитайте массу серной кислоты, которая взаимодействует с 5,6 г гидроксида калия. В результате реакции образуется сульфат калия и вода.
ДАНО:
m(____) = 5,6 г
РЕШЕНИЕ:
1) H2SO4 + 2К0Н = K2SO4 + 2Н2О.
2) n(КОН)= 5,6 г : 56г/моль = 0,1 моль.
3) H2SO4 + 2КОН = K2SO4 + 2Н2О.
4) n(H2SO4): n(KOH) = 1:2 (по уравнению) n(H2SO4) = 0,5«(KOH) = 0,5 x 0,1 моль = 0,05 моль.
m(H2SO4) - 0,05 моль • _ г/моль = г.
Часть II
1. Заполните пропуски, проанализировав уравнение реакции.
4Р + 5О2 = 2Р2О6
Число частиц, N
Количество вещества, n
Молярная масса, М
Масса, m
Молярный объём, Vm
Объём, V—
1) Если в реакцию вступит 3 моль фосфора, то потребуется моль кислорода, и образуется моль оксида фосфора (V).
2) Для получения 213 г оксида фосфора (V) необходимо _ л кислорода и _ г фосфора.
3) Из _ г фосфора при взаимодействии с 11,2 л кислорода образуется _ г оксида фосфора (V).
1) Если в реакцию вступит 3 моль фосфора, то потребуется 3,75 (3·5/4=3,75) моль кислорода, и образуется 1,5 моль (3,75·2/5=1,5) оксида фосфора (V).
2) Для получения 218 г оксида фосфора (V) необходимо 86 л (112·218/284=86) кислорода и 95 г (124·218/284=95) фосфора.
3) Из 12,4 г (11,2·124/112=12,4) фосфора при взаимодействии с 11,2 л кислорода образуется 28,4 г (11,2·284/112=28,4) оксида фосфора (V).
2. Рассчитайте массу магния, который может сгореть в кислороде объёмом 33,6 л (н. у.). Схема химической реакции:
Mg + O2 — > MgO.
1-й способ
2-й способ
2) Составьте и решите пропорцию
Похожие решебники
Популярные решебники 8 класс Все решебники
*размещая тексты в комментариях ниже, вы автоматически соглашаетесь с пользовательским соглашением






