Часть ll Параграф 28 ГДЗ Рабочая тетрадь Габриелян Остроумов 8 класс (Химия)
Решение #1

Рассмотрим вариант решения задания из учебника Габриелян, Остроумов, Сладков 8 класс, Просвещение:
Часть II
1. Выберите верное утверждение.
1) Классификация Берцелиуса верна, так как её полностью подтверждают рассмотренные ранее генетические ряды металлов
и неметаллов.
2) Классификация Берцелиуса относительна (не совсем верна).
Аргументируйте свой ответ.
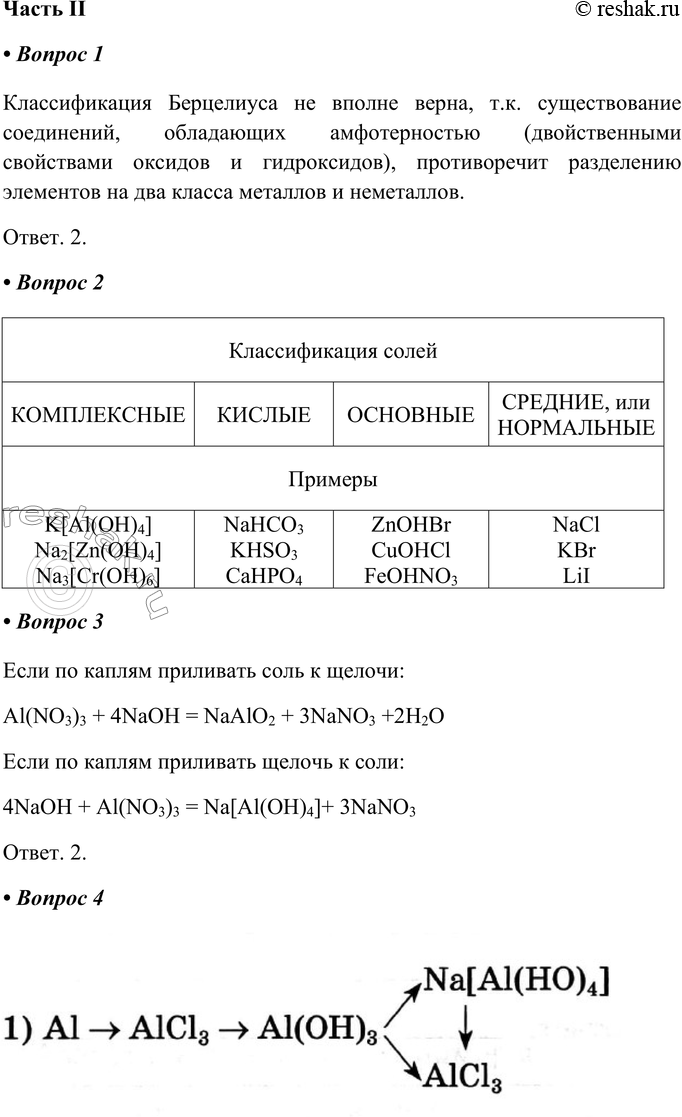
Классификация Берцелиуса не вполне верна, т.к. существование соединений, обладающих амфотерностью (двойственными свойствами оксидов и гидроксидов), противоречит разделению элементов на два класса металлов и неметаллов.
Ответ. 2.
2. Оформите схему.
Классификация солей
Примеры
3. Выберите верное утверждение.
1) Для получения амфотерного гидроксида нужно по каплям приливать к раствору щёлочи раствор соли.
2) Для получения амфотерного гидроксида нужно по каплям приливать к раствору соли раствор щёлочи.
Подтвердите ответ уравнениями реакций.
Если по каплям приливать соль к щелочи:
Al(NO3)3 + 4NaOH = NaAlO2 + 3NaNO3 +2H2O
Если по каплям приливать щелочь к соли:
4NaOH + Al(NO3)3 = Na[Al(OH)4]+ 3NaNO3
Ответ. 2.
4. Напишите уравнения реакций следующих превращений:
1) 2Al + 3Cl2 = 2AlCl3
AlCl3 + 3KOH = Al(OH)3 + 3KCl
NaOH + Al(OH)3= Na[Al(OH)4]
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Na[Al(OH)4] + 4HCl = AlCl3 + NaCl + 4H2O
2) 2Zn + O2 = 2ZnO
ZnO + SO3 = ZnSO4
ZnSO4 + Ba(OH)2 = BaSO4 + Zn(OH)2
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4]
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
Na2[Zn(OH)4] + 2H2SO4 = Na2SO4 + ZnSO4 + 4H2O
5. Рассчитайте количество вещества гидроксида натрия, необходимого для перевода 483 г 10%-ного раствора сульфата цинка в сульфат натрия согласно уравнению
ZnSO4 + 4NaOH = Na2SO4 + Na2ZnO2 + 2H2O
Рассчитайте количество выделившейся воды.
Дано:
m(раствора ZnSO4)=483 г
w(ZnSO4)=10%
M(ZnSO4)= 161 г/моль
m(ZnSO4)= m(раствора ZnSO4) · w(ZnSO4)/100%= 483·0,1=48,3 (г)
n(ZnSO4)=m/M=48,3 /161= 0,3 (моль)
По уравнению реакции:
ZnSO4 NaOH H2O
0,3моль x моль x моль
1 молекула 4 молекулы 2 молекулы
x=n(NaOH)= 0,3·4/1=1,2 (моль)
y=n(H2O)= 0,3·2/1=0,6 (моль)
Ответ. 1,2 моль, 0,6 моль.
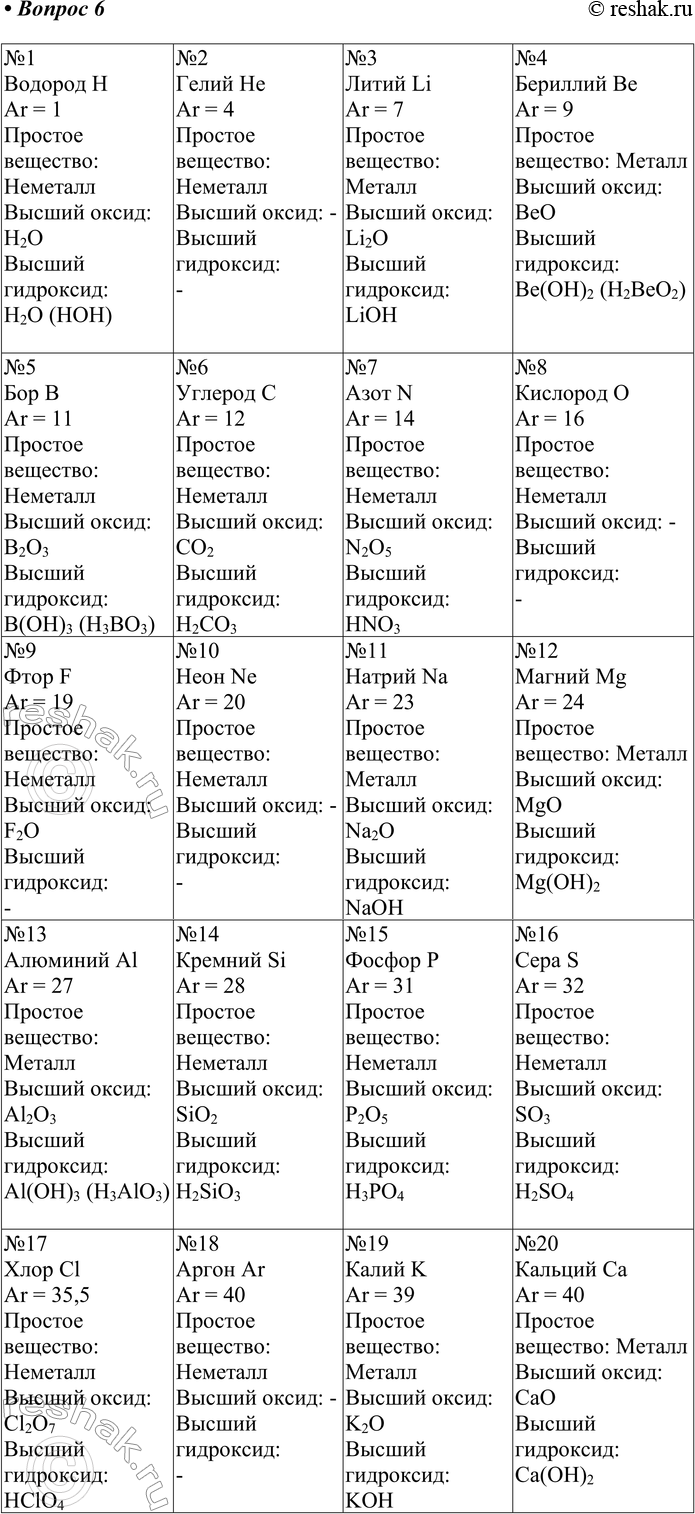
6. Подготовьте 20 карточек для лабораторной работы к § 29. На них напишите символы первых 20 химических элементов с указанием относительной атомной массы, характера простого вещества (металл или неметалл), формулы высших оксида и гидроксида (основания, кислородсодержащей кислоты или амфотерного гидроксида).
Похожие решебники
Популярные решебники 8 класс Все решебники
*размещая тексты в комментариях ниже, вы автоматически соглашаетесь с пользовательским соглашением






